CSL Behring presenta solicitud de licencia de producto biológico para aprobación de la inmunoglobulina humana subcutánea
CSL Behring ha presentado una solicitud de licencia de producto biológico (BLA en sus siglas en inglés) a la Agencia de Alimentos y Fármacos de EE.UU. (USFDA en sus siglas en inglés) solicitando la aprobación para comercializar su formulación líquida al 20% de la inmunoglobulina subcutánea (humana) (IgSc en sus siglas en inglés), en Estados Unidos como terapia de sustitución semanal en pacientes con inmunodeficiencias primarias.
Noticias más leídas
Más noticias del departamento investigación y desarrollo

Reciba la química en su bandeja de entrada
Al enviar el formulario, se muestra usted de acuerdo con que LUMITOS AG le envíe por correo electrónico el boletín o boletines seleccionados anteriormente. Sus datos no se facilitarán a terceros. El almacenamiento y el procesamiento de sus datos se realiza sobre la base de nuestra política de protección de datos. LUMITOS puede ponerse en contacto con usted por correo electrónico a efectos publicitarios o de investigación de mercado y opinión. Puede revocar en todo momento su consentimiento sin efecto retroactivo y sin necesidad de indicar los motivos informando por correo postal a LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlín (Alemania) o por correo electrónico a revoke@lumitos.com. Además, en cada correo electrónico se incluye un enlace para anular la suscripción al boletín informativo correspondiente.
Noticias más leídas
Más noticias de nuestros otros portales
Contenido visto recientemente
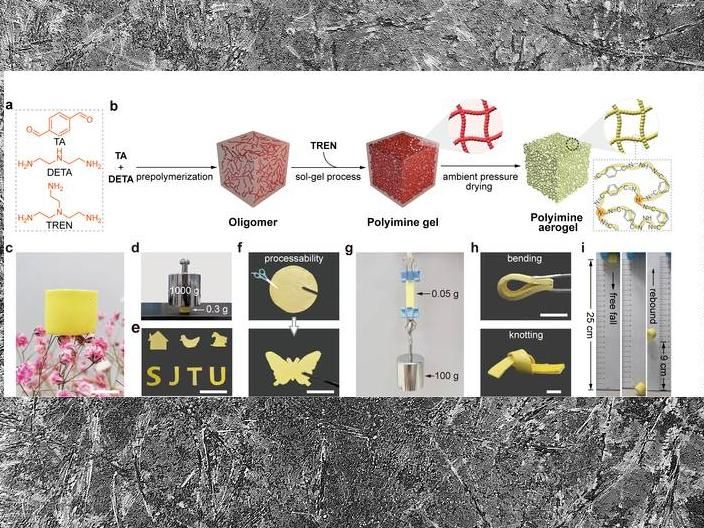
Aerogeles monolíticos de polímeros covalentes dinámicos con capacidad de reciclaje en circuito cerrado

SCHWING Technologies GmbH - Neukirchen-Vluyn, Alemania

Altenburger Maschinen Jäckering GmbH - Hamm, Alemania