Reacción vicinal: Una estrategia radical para vincular a tres grupos orgánicos
Los químicos orgánicos son arquitectos moleculares que diseñan estructuras sofisticadas. A medida que las moléculas utilizadas en la ciencia y la medicina se vuelven cada vez más complejas, se necesitan nuevas herramientas para unir los bloques de construcción. Ahora, un equipo japonés de la Universidad de Kanazawa ha desarrollado una reacción que une tres componentes a la vez utilizando la química de los radicales libres.

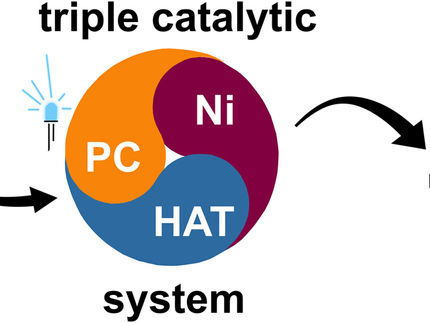
Un equipo de investigación japonés de la Universidad de Kanazawa desarrolló una reacción para crear cetonas funcionalizadas. Utilizando un organocatalizador de N-heterocyclic carbene (NHC), sin necesidad de metales o irradiación ligera, se añaden un acilo y un grupo alquilo a través del enlace doble de un alqueno. El NHC da control regioselectivo sobre un proceso de retransmisión que implica la transferencia de electrones seguida de la adición sucesiva de dos radicales en el alqueno. Los diversos productos son bloques de construcción útiles para posteriores síntesis.
Kanazawa University
Los enlaces dobles carbono-carbono, conocidos como alcanos, son más reactivos que los enlaces simples. Esto los hace útiles para conectar diferentes grupos: si se rompe el doble enlace, se pueden añadir dos nuevas moléculas en cada extremo, unidas entre sí por el antiguo alqueno, ahora de enlace simple.
El equipo de Kanazawa estudió la forma de lograr esta transformación utilizando aldehídos, que contienen un doble enlace entre el oxígeno y el carbono, como una de las dos moléculas injertadas en un alqueno. Como se informó en el Journal of the American Chemical Society, el objetivo era crear cetonas altamente funcionalizadas, una familia importante de compuestos en la síntesis orgánica.
Su método elegido fue una reacción conocida, suficientemente evocativa, como una retransmisión radical. Los radicales (o radicales libres) que contienen un electrón no emparejado, y por lo tanto una órbita semivacía, tienden a ser vorazmente reactivos. Tan reactivos, de hecho, que no pueden ser almacenados, sino que deben ser generados in-situ por medio del látigo de un electrón de algún lugar durante una reacción, provocando una cascada de rompimiento y formación de enlaces.
Los químicos pueden hacer radicales de varias maneras, pero el equipo de Kanazawa quería hacer pruebas de carretera con oraganocatalizador, llamado N-heterocyclic carbene (NHC). Con un aldehído como un reactante y un éster redox funcionalizado como el otro, el NHC desencadenó su transformación en radicales. Estudios previos insinuaron que ambos radicales reaccionarían más rápido con un alqueno que entre sí.
"El desafío con los radicales es que, al ser tan inestables, a menudo reaccionan consigo mismos", dice Kazunori Nagao, coautor del estudio. "Luego se recuperan los materiales de partida, o un producto secundario, en lugar del objetivo. Hemos minimizado esto aquí. De hecho, la reacción procedió como un relé - primero el radical alquílico añadido a un carbono del alqueno, y luego el radical acílico añadido al otro".
El compuesto resultante tenía una cetona y un grupo derivado de éster unidos a dos carbones adyacentes, en una disposición denominada vicinal. Aunque también se produjo una reacción directa entre los diferentes radicales, lo que dio como resultado un producto no deseado de dos componentes, en lugar del objetivo de tres componentes puenteado con alkene-, fue menor. Además, una amplia gama de materiales de partida eran compatibles con el proceso.
"Vale la pena mencionar dos puntos cruciales", dice Hirohisa Ohmiya, autora correspondiente del estudio. "Primero, a diferencia de algunas reacciones, la nuestra está libre de catalizadores metálicos y no necesita una fuente de luz para producir radicales, lo que la hace verde y versátil. En segundo lugar, el NHC controla con precisión el relé, por lo que podemos ser selectivos en las posiciones de los grupos funcionales. Estamos trabajando en una versión asimétrica para productos quimicos".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.