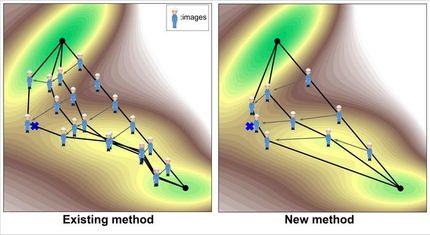
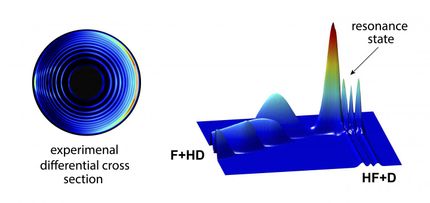
¿La reacción química más simple es realmente tan simple?
El mecanismo descubierto conduce a una clara interferencia cuántica y verifica que la Naturaleza "juega a los dados"
La mayoría de la gente piensa que la teoría cuántica, que describe el movimiento de las moléculas y las partículas atómicas y subatómicas, es contraria a la intuición, ya que la mecánica cuántica describe un comportamiento que está en desacuerdo con la mecánica clásica. Incluso Albert Einstein, que nunca aceptó la mecánica cuántica, dijo famosamente que "Él (Dios o la Naturaleza) no juega a los dados" - lo que significa que las leyes de la física no se rinden ante la incertidumbre o el azar como implica la teoría cuántica.
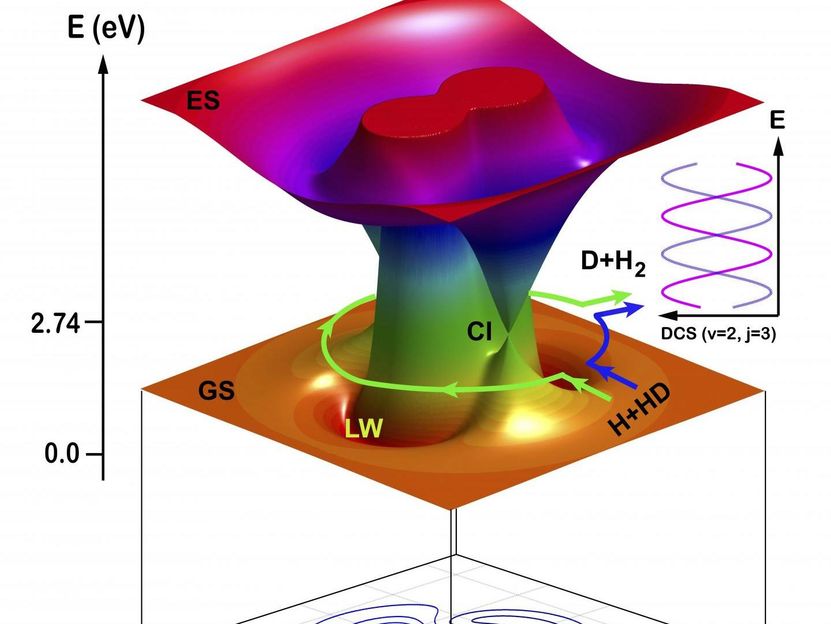
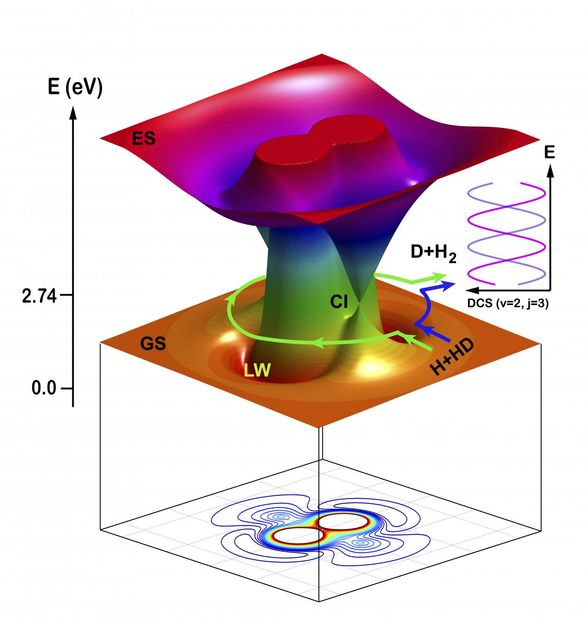
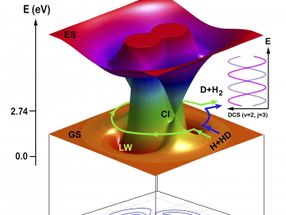
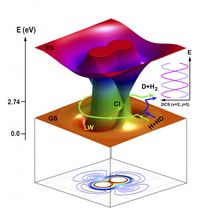
Ilustración esquemática de las dos vías topológicas de la reacción H + HD a H2 + D: la vía de reacción de abstracción directa (en sentido contrario a las agujas del reloj) y la vía de reacción de inserción itinerante (en sentido de las agujas del reloj).
DICP
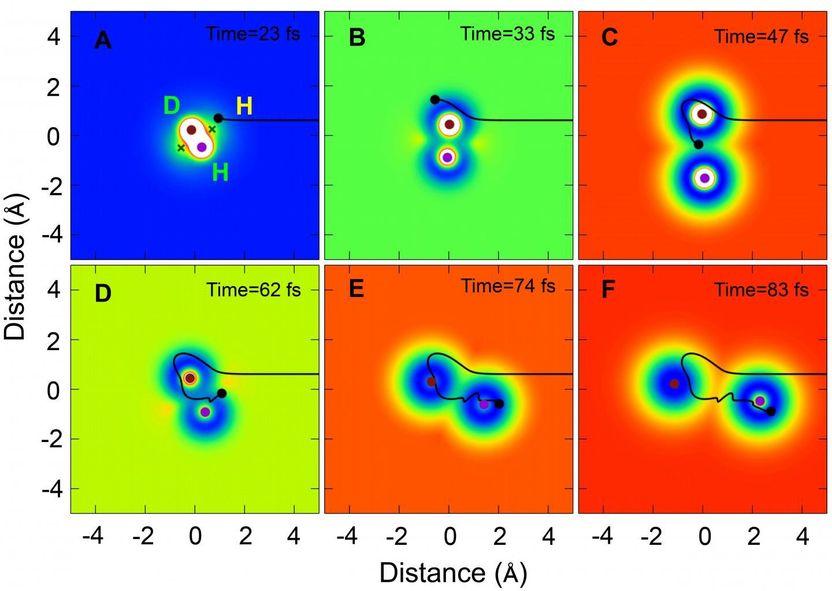
Una trayectoria representativa de la reacción H + HD a H2 + D en cierto ángulo de dispersión (dirección de dispersión hacia atrás) a través del mecanismo de itinerancia que se mueve con el tiempo en coordenadas cartesianas.
DICP
Una reacción química a veces se produce de una manera extraña, ya que en la vista microscópica el progreso de una reacción se rige por la teoría cuántica.
Las nuevas investigaciones de los científicos del Instituto de Física Química de Dalian (DICP) de la Academia China de Ciencias (CAS) han demostrado, sorprendentemente, que en la reacción más simple y bien estudiada, todavía hay un mecanismo no descubierto. Conduce a una clara interferencia cuántica y verifica nuevamente que la Naturaleza "juega a los dados".
La reacción en cuestión es H + HD → H2 + D. En el estudio, publicado en Science el 15 de mayo, los grupos dirigidos por los Profs. YANG Xueming, ZHANG Donghui, SUN Zhigang y XIAO Chunlei del DICP descubrieron un nuevo tipo de interferencia cuántica en esta simple reacción.
En la física, la interferencia es la combinación de dos o más formas de onda para formar una onda resultante, en la que el desplazamiento se refuerza o se cancela. La interferencia cuántica puede ocurrir entre partículas que llegan a la misma posición o estado cuántico pero por caminos diferentes.
Dado que una reacción química es esencialmente un proceso de colisión y dispersión en el que participan átomos y/o moléculas, podemos esperar que se produzcan fenómenos de interferencia en una reacción química.
Entre todas las reacciones químicas, la reacción H + H2 y sus isótopos son las más simples. Esta reacción sólo involucra tres electrones; por lo tanto, es conveniente tratar con la química cuántica precisa para calcular la energía de interacción que involucra a los tres átomos.
El año pasado, los investigadores del DICP encontraron oscilaciones fuertes y regulares en función de la energía en cierto ángulo de dispersión del producto H2 durante la reacción H + HD en estados de rovibración particulares.
En realidad, se han observado oscilaciones similares en otras reacciones, pero no son tan regulares como las de la reacción H + HD. El origen físico de tales oscilaciones sigue sin estar claro.
Para entender este interesante fenómeno, los investigadores realizaron un estudio teórico y experimental combinado de la reacción H + HD.
Experimentalmente, al mejorar el aparato de haz molecular cruzado, registraron señales de dispersión reactivas con cierto ángulo de dispersión en función de la alta energía relativa.
Desarrollaron aún más los métodos de dinámica cuántica aplicando la teoría topológica para analizar los caminos a través de los cuales procedía la reacción. La teoría topológica reveló que las oscilaciones regulares observadas eran el resultado de la interferencia entre productos generados por dos caminos diferentes.
Los investigadores analizaron los mecanismos dinámicos de la reacción utilizando la teoría de la trayectoria cuasiclásica (QCT). Los resultados mostraron que la reacción procedía por una vía utilizando el mecanismo tradicional de extracción directa, es decir, el átomo de H entrante chocaba con el átomo de H en la molécula de reactivo diatómico HD y lo extraía para formar un nuevo enlace químico de H2.
La reacción también procedió por otro camino utilizando un nuevo mecanismo de itinerancia. Las instantáneas de la teoría QCT para el mecanismo de itinerancia muestran que el átomo de H entrante se acercó inicialmente a la molécula de HD a través de la región de intersección cónica (Cl) en la dirección del extremo del átomo D, y luego vagó alrededor del átomo D en HD. Cuando el átomo de H entrante se acercó a la región CI, el enlace HD comenzó a estirarse, haciendo posible que el átomo de H errante se insertara en la molécula HD estirada. El átomo de H entrante formó entonces un nuevo enlace químico con el átomo de H en la EH.
Los productos (H2) de estos dos caminos se dispersaron en el mismo ángulo de dispersión, donde se produjo una interferencia cuántica.
Además, la probabilidad de que ocurra un mecanismo de rovibración tan inusual es bastante baja - sólo alrededor del 0,3% de todas las reacciones.
Este trabajo demuestra una vez más la naturaleza cuántica de una reacción química a nivel microscópico. También revela que las reacciones químicas son complicadas.
Incluso la simple reacción H + HD → H2 + D, que se ha estudiado durante décadas, tiene una pequeña probabilidad de emplear mecanismos inesperados.
En la vida, muchos grandes eventos son desencadenados por eventos de pequeña probabilidad. ¿Quién puede garantizar que un mecanismo de reacción de tan pequeña probabilidad no conduzca a resultados sorprendentes?
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.