Especies activas de platino
Oxidaciones catalíticas a alta temperatura: ¿Átomo individual o grupo de metales?
Los catalizadores de platino altamente dispersos ofrecen nuevas posibilidades para los procesos industriales, como la combustión sin llama de metano, propano o monóxido de carbono, que tiene menos emisiones y es más eficiente en cuanto a recursos y consistente que la combustión convencional. En la revista Angewandte Chemie, un equipo de investigadores informa sobre qué especies de platino son activas en oxidaciones a alta temperatura y qué cambios pueden sufrir en el transcurso del proceso, requisitos importantes para la optimización de los catalizadores.
© Wiley-VCH
Los átomos de metal individuales y los clusters formados por unos pocos átomos de metal tienen interesantes propiedades catalíticas determinadas por la naturaleza exacta de las especies metálicas activas. Por lo general, éstas están muy dispersas y se depositan sobre un soporte como la zeolita, que es una estructura de marco de silicato poroso que también desempeña un papel en las características de un catalizador. Incluso el más mínimo cambio en los centros activos puede reducir drásticamente la eficacia de un catalizador. Por ejemplo, los metales nobles como el platino tienden a desactivarse permanentemente por sinterización en condiciones duras.
Sin embargo, es difícil determinar qué especies específicas de platino desempeñan un papel en las oxidaciones a alta temperatura, porque un número significativo de estas especies no puede obtenerse fácilmente sin la participación de su soporte en la catálisis. Un equipo dirigido por Pedro Serna (ExxonMobil Research and Engineering Co., Nueva Jersey, EE.UU.), así como por Manuel Moliner y Avelino Corma (Universitat Politècnica de València, España) investigó el comportamiento de los átomos individuales de platino y de los pequeños cúmulos de platino sobre zeolitas especiales CHA, que son soportes no reducibles que pueden estabilizar muy bien estas especies.
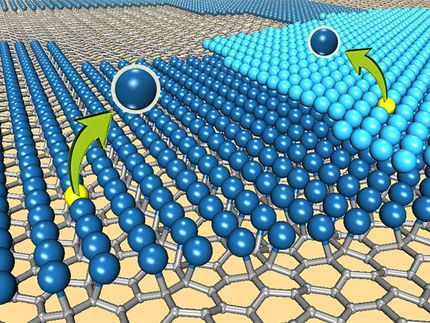
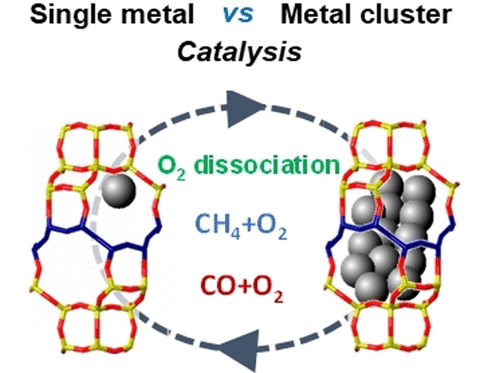
Su primer experimento fue una investigación sobre la división del O2 utilizando dos tipos diferentes de moléculas de oxígeno isotópicamente puras, 16O2y 18O2. Cuanto más activo es el catalizador, más moléculas 16O18Omezcladas se forman al recombinar los átomos disociados. Se demostró que las agrupaciones de platino de menos de un nanómetro son significativamente más activas que los átomos individuales o las agrupaciones más grandes. Sin embargo, a temperaturas moderadas (200 °C) los diminutos grupos se desintegran con el tiempo en átomos individuales de platino y la actividad catalítica para dividir el oxígeno termina.
En cambio, el equipo descubrió que para la oxidación de alcanos, como el metano, a temperaturas más elevadas, la combustión catalítica corría a cargo de átomos de platino individuales. Éstos se forman in situ en la corriente de oxígeno a partir de las agrupaciones iniciales, como se demostró por espectroscopia de absorción de rayos X y por microscopía electrónica. El paso crítico en estas oxidaciones no es el desdoblamiento del O2 sino la ruptura de los enlaces C-H, que es menos sensible a los cambios en la estructura del sitio activo.
En la oxidación del CO, la catálisis está dominada por los grupos de platino. Los átomos de platino individuales no pueden estabilizarse en la corriente de CO y, por tanto, no desempeñan ningún papel. En comparación con los soportes de óxido de aluminio, la zeolita CHA proporcionó una mayor actividad y una mayor estabilidad de los clusters de platino en presencia de CO.
La alta estabilidad de los átomos de platino individuales para la combustión de metano y de los pequeños clusters de platino para la oxidación de CO, que se mantiene tras la regeneración o el tratamiento con vapor caliente, abre nuevas posibilidades para los sistemas hechos de zeolitas de platino y silicato como catalizadores heterogéneos eficientes y robustos para una variedad de escenarios de oxidación a alta temperatura.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.