Importante hito en el camino hacia la catálisis de metales de transición con aluminio
Químicos sintetizan con éxito una sal catiónica de complejo de aluminio de bajo valor mediante metátesis
Los químicos Philipp Dabringhaus, Julie Willrett y el Prof. Dr. Ingo Krossing del Instituto de Química Inorgánica y Analítica de la Universidad de Friburgo han logrado sintetizar el complejo de aluminio catiónico de bajo valor [Al(AlCp*)3]+ mediante una reacción de metátesis. El equipo presenta su trabajo de investigación en la revista Nature Chemistry.
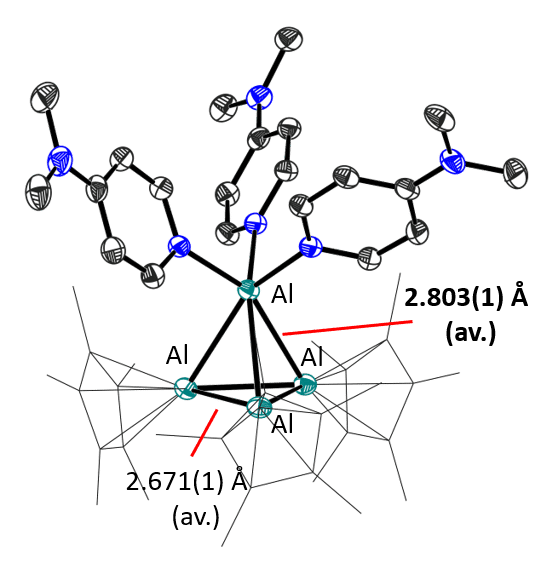
La adición de ligandos, como la dimetilaminopiridina en este caso, rompe la estructura dimérica del catión y el átomo solitario de aluminio muestra su fuerte carácter aceptor.
Image: provided by the research group
"En química, los compuestos catiónicos de aluminio de bajo valor son muy buscados debido a su potencial reactividad ambifílica similar a la de los metales de transición. Sin embargo, numerosos intentos anteriores de sintetizar compuestos catiónicos de aluminio de bajo valor por métodos oxidativos o reductores han sido en gran medida infructuosos", explica Krossing. Hasta ahora, dijo, sólo ha habido un ejemplo de un compuesto de aluminio catiónico de bajo valor, pero no se puede preparar por síntesis racional. "Ahora demostramos que, después de todo, hay un acceso inesperadamente fácil a los complejos de aluminio de bajo valor con la metátesis", dice Krossing. En la metátesis, simplemente se intercambian estructuras parciales entre los socios de la reacción.
El aluminio como alternativa más barata para la catálisis
Los químicos de Friburgo prepararon la sal [Al(AlCp*)3]+[Al(OC{CF3)3}4]- a partir del tetrámero de Schnöckel (AlCp*)4, en el que el aluminio ya está presente en el estado de oxidación +1. El (AlCp*)4 reaccionó con Li[Al{OC(CF3)3}4] y la mezcla de reacción pasó inmediatamente del amarillo al rojo. Cuando la mezcla de reacción se cristalizó, los científicos obtuvieron la sal [Al(AlCp*)3]+[Al(OC{CF3)3}4] como cristales de color morado oscuro. "Los estudios cristalográficos de rayos X, de espectrometría UV y computacionales indican la presencia de la estructura dimérica tanto en estado sólido como en solución a alta concentración y baja temperatura, pero a baja concentración y temperatura ambiente se forma el monómero. Esto indica claramente la reactividad ambifílica del catión", dijo Dabringhaus.
"En consecuencia, esta sal puede utilizarse potencialmente como bloque de construcción para una sal [:Al(L)3]+ que, debido a su naturaleza catiónica, podría ser capaz de realizar adiciones oxidativas reversibles y eliminaciones reductoras de pequeñas moléculas", explica Krossing. "Esto nos acerca un poco más a nuestro objetivo a largo plazo de conseguir la catálisis -que actualmente se realiza con metales de transición caros y raros- con aluminio". El aluminio es el segundo elemento más abundante en la corteza terrestre y es capaz de hacerlo en principio, como demuestra nuestro trabajo. Pero, por desgracia, probablemente pasarán al menos otros 20 años antes de que se aplique nuestra investigación al respecto".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Noticias más leídas
Más noticias del departamento ciencias

Reciba la química en su bandeja de entrada
Al enviar el formulario, se muestra usted de acuerdo con que LUMITOS AG le envíe por correo electrónico el boletín o boletines seleccionados anteriormente. Sus datos no se facilitarán a terceros. El almacenamiento y el procesamiento de sus datos se realiza sobre la base de nuestra política de protección de datos. LUMITOS puede ponerse en contacto con usted por correo electrónico a efectos publicitarios o de investigación de mercado y opinión. Puede revocar en todo momento su consentimiento sin efecto retroactivo y sin necesidad de indicar los motivos informando por correo postal a LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlín (Alemania) o por correo electrónico a revoke@lumitos.com. Además, en cada correo electrónico se incluye un enlace para anular la suscripción al boletín informativo correspondiente.
Noticias más leídas
Más noticias de nuestros otros portales
Contenido visto recientemente
Tiopentato_de_sodio

SKW Stickstoffwerke Piesteritz GmbH - Lutherstadt Wittenberg, Alemania

AAE Chemie N.V. - Kalmthout, Bélgica