Por qué las cavidades ópticas frenan la velocidad de las reacciones químicas
"Este trabajo sitúa el controvertido campo de la química polaritónica en otro nivel"
Los procesos químicos nos rodean. Desde nuevos materiales hasta medicamentos o productos plásticos más eficaces, las reacciones químicas desempeñan un papel fundamental en el diseño de las cosas que usamos a diario. Los científicos buscan constantemente mejores formas de controlar estas reacciones, por ejemplo para desarrollar nuevos materiales. Ahora, un equipo internacional de investigación dirigido por el MPSD ha hallado una explicación de por qué las reacciones químicas se ralentizan en el interior de cavidades espejadas, donde las moléculas se ven obligadas a interactuar con la luz. Su trabajo, publicado en Nature Communications, es un paso clave para comprender este proceso observado experimentalmente.
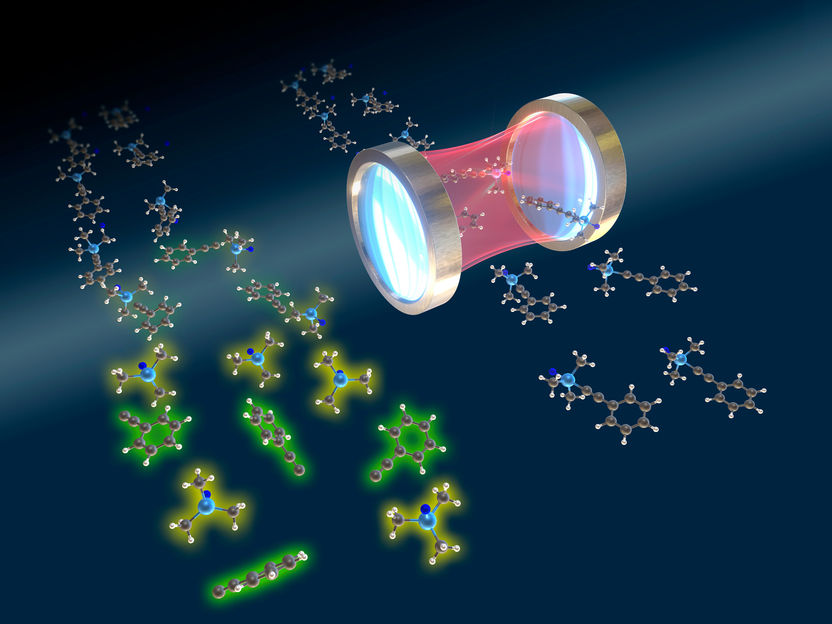
El fuerte acoplamiento vibracional resonante puede inhibir reacciones químicas. El acoplamiento resonante fuerte entre la cavidad y los modos vibracionales puede inhibir selectivamente una reacción química.
E. Ronca / C. Schäfer
Las reacciones químicas se producen a escala de vibraciones atómicas, un millón de veces más pequeñas que el grosor de un cabello humano. Estos minúsculos movimientos son difíciles de controlar. Los métodos establecidos incluyen el control de la temperatura o el suministro de superficies y complejos en disolución hechos de materiales poco comunes. Abordan el problema a mayor escala y no pueden dirigirse a partes específicas de la molécula. Idealmente, los investigadores querrían proporcionar sólo una pequeña cantidad de energía a algunos átomos en el momento adecuado, igual que un jugador de billar quiere empujar sólo una bola sobre la mesa.
En los últimos años, se ha puesto de manifiesto que las moléculas experimentan cambios fundamentales cuando se colocan en cavidades ópticas con espejos opuestos. Dentro de esos confines, el sistema se ve obligado a interactuar con luz virtual, o fotones. Esta interacción modifica la velocidad de las reacciones químicas, un efecto que se ha observado en experimentos pero cuyo mecanismo subyacente sigue siendo un misterio.
Ahora, un equipo de físicos teóricos de Alemania, Suecia, Italia y EE.UU. ha dado con una posible explicación, que coincide cualitativamente con los resultados experimentales. En el equipo participaron investigadores del Instituto Max Planck de Estructura y Dinámica de la Materia (MPSD) de Hamburgo (Alemania), la Universidad Tecnológica de Chalmers (Suecia), el Centro de Física Cuántica Computacional del Flatiron Institute de la Universidad de Harvard (ambos en EE.UU.) y el Istituto per i Processi Chimico Fisici del CNR (Consejo Nacional de Investigación) de Italia.
Utilizando un método teórico avanzado, denominado Teoría Cuántica-Electrodinámica del Funcional de la Densidad (QEDFT), los autores han desvelado el mecanismo microscópico que reduce la velocidad de reacción química, para el caso concreto de la reacción de desprotección del 1-fenil-2-trimetilsililacetileno. Sus hallazgos concuerdan con las observaciones del grupo de Thomas Ebbesen en Estrasburgo.
El equipo descubrió que las condiciones dentro de la cavidad óptica afectan a la energía que hace vibrar los átomos alrededor de los enlaces simples de la molécula, que son críticos para la reacción química.
Fuera de la cavidad, esa energía suele depositarse en un enlace simple durante la reacción, lo que en última instancia puede romper el enlace, un paso clave en una reacción química. "Sin embargo, descubrimos que la cavidad introduce una nueva vía, de modo que es menos probable que la energía se canalice hacia un único enlace", explica Christian Schäfer, autor principal. "Éste es el proceso clave que inhibe la reacción química, porque disminuye la probabilidad de romper un enlace específico".
La manipulación de materiales mediante el uso de cavidades (la llamada "química polaritónica") es una poderosa herramienta con muchas aplicaciones potenciales, según el autor del artículo Enrico Ronca, que trabaja en el CNR: "Por ejemplo, se observó que el acoplamiento a excitaciones vibracionales específicas puede inhibir, dirigir e incluso catalizar un proceso químico a temperatura ambiente. Nuestro trabajo teórico mejora la comprensión de los mecanismos microscópicos subyacentes para el caso específico de una reacción inhibida por el campo."
Aunque los autores señalan que aún quedan aspectos importantes por comprender y que es necesaria una mayor validación experimental, también destacan el papel especial de esta nueva dirección. "Este trabajo sitúa el controvertido campo de la química polaritónica en otro nivel", añade Ángel Rubio, Director del Departamento de Teoría del MPSD. "Aporta conocimientos fundamentales sobre los mecanismos microscópicos que permiten controlar las reacciones químicas. Esperamos que los presentes hallazgos puedan aplicarse a un conjunto más amplio de reacciones relevantes (incluidas las reacciones químicas clic vinculadas al Premio Nobel de Química de este año) en condiciones de fuerte acoplamiento luz-materia."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.