Química por la fuerza
¿Cómo desencadenar una reacción química sin utilizar disolventes?
Botella, tubo de cristal y disolvente, eso es lo que solemos encontrar en un laboratorio de química o en la industria. La química que utiliza disolventes, o materiales de base líquida, es la forma tradicional de síntesis. Aunque es muy eficaz, una pregunta inevitable es cómo reciclar el disolvente de forma segura y respetuosa con el medio ambiente. La respuesta más sencilla es la química sin disolventes, pero ¿cómo desencadenar una reacción química sin utilizar disolventes?

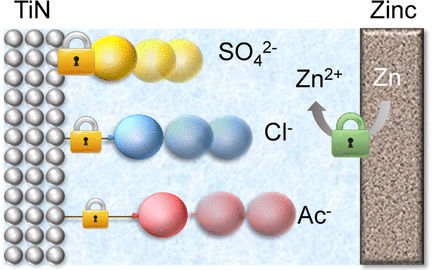
Figura esquemática de AgI comprimido.
Qingyang Hu
En 1820, Michael Faraday aportó su idea utilizando la fuerza bruta, en la que utilizó la trituración en un mortero para inducir la reducción mecánica de AgCl con Zn, Sn, Fe y Cu. Este es probablemente el primer experimento de la llamada mecanoquímica. Por definición, la mecanoquímica convierte directamente la energía mecánica en energía química, o potencial químico. La molienda mecánica es la forma más común de realizar la mecanoquímica. Pero la fuerza aplicada por la molienda manual es limitada y, por tanto, muchos materiales son químicamente estables bajo un proceso mecánico tan suave. Aquí, un trabajo en el que colaboran la Universidad de Yantai, HPSTAR, la Universidad de Linyi, ESRF y la Universidad Estatal de California Northbridge, utiliza un par de diamantes para comprimir polvos de AgI a presiones extremadamente altas, equivalentes a 420.000 atmósferas. Observaron la descomposición de AgI en los miembros elementales de Ag e I.
"Nos interesa el AgI porque se informó de que es un sólido superiónico a alta temperatura, en el que la plata es un sólido y el yodo se comporta como líquido. Esto es útil para fabricar electrolitos de baterías", explica Jianfu Li, de la Universidad de Yantai. "No se produce ninguna química entre el cristal ordinario y el sólido superiónico. Pero si aumentamos la presión lo suficiente, los iones Ag e I se movilizan y empiezan a reaccionar".
El experimento de alta presión se realizó en la Instalación Europea de Radiación Sincrotrón, donde los científicos pueden utilizar rayos X focalizados de alta energía para medir la estructura de las muestras en esas condiciones de presión. Observaron claramente la desaparición del sólido AgI y la aparición de Ag e I. "Cada enlace tiene su propio límite químico. En este sólido superiónico, hemos alcanzado el límite químico del AgI aplicando presión. Más allá de este límite, observamos la descomposición y el colapso de la ionicidad", añadió Qingyang Hu, científico del HPSTAR. "Esta química inducida por la presión también debería producirse en otros sólidos iónicos como AgCl y AgBr, pero a presiones aún mayores".
El experimento fue pionero en la modelización computacional, en la que se predice la evolución del enlace Ag-I y sus propiedades a altas presiones. "Somos capaces de predecir la estructura estable de AgI en las condiciones de presión pertinentes mediante el denominado algoritmo de búsqueda estructural. Este es otro ejemplo que demuestra la capacidad de este algoritmo", explicó el profesor Xiaoli Wang. "Mediante el seguimiento de las propiedades iónicas del AgI, cada paso de esta mecanoquímica se demuestra teóricamente y se exhibe perfectamente en nuestro experimento. Nuestro enfoque computacional posiblemente pueda diseñar nuevos caminos para las reacciones químicas".
Este trabajo se publica en el Journal of American Chemical Society Au como artículo de portada.
Más información: "Mechanochemistry and the Evolution of Ionic Bonds in Dense Silver Iodide", Li et al., JACS Au 2023.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.