Dos conductores de una reacción química
Ver la reacción en directo
Por primera vez, investigadores de la Universidad Técnica de Viena han logrado observar en tiempo real el principio de funcionamiento de los llamados promotores en una reacción catalítica. Estos promotores desempeñan un importante papel en la tecnología, pero hasta ahora sólo se conoce de forma limitada cómo funcionan.
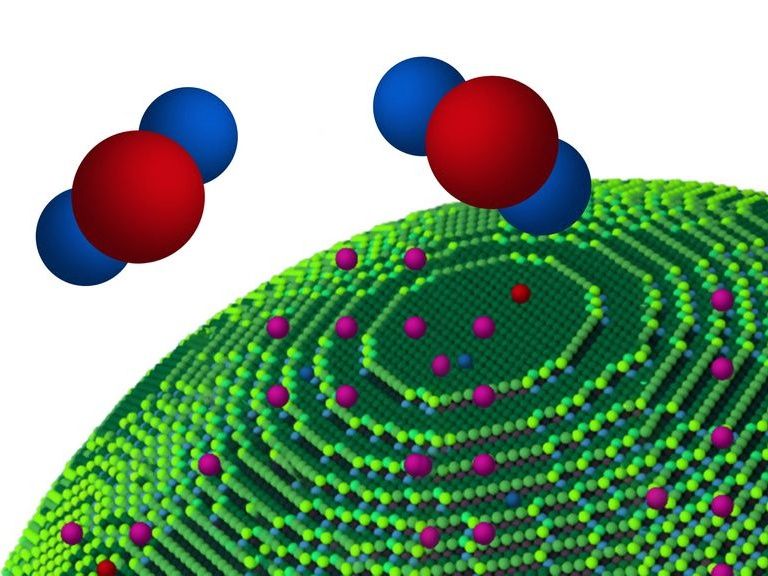
Moléculas de agua delante de la nanopartícula
TU Wien
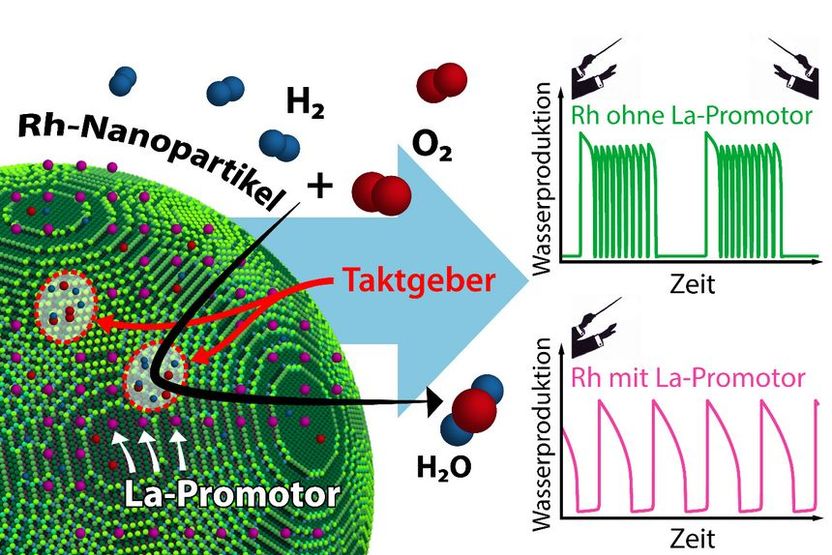
El comportamiento de reacción de una nanopartícula individual viene determinado por sus marcapasos. La adición de un promotor La influye significativamente en la interacción de estos marcapasos.
TU Wien
Los catalizadores son esenciales para numerosas tecnologías químicas, desde la purificación de gases de escape hasta la producción de valiosos productos químicos y vectores energéticos. A menudo se utilizan pequeñas trazas de sustancias adicionales junto a los catalizadores para hacerlos más eficaces. Estas sustancias se denominan "promotores". Aunque desempeñan un papel crucial en la tecnología, han sido notoriamente difíciles de estudiar.
En la mayoría de los casos, determinar qué cantidad de promotores tiene qué efectos sobre un catalizador ha sido un proceso de ensayo y error. Sin embargo, los investigadores de la Universidad Técnica de Viena han conseguido observar directamente el papel de los promotores de lantano en la oxidación del hidrógeno. Utilizando métodos de microscopía de alta tecnología, visualizaron el papel de los átomos individuales de La. Su estudio reveló que dos áreas superficiales del catalizador actúan como marcapasos, de forma similar a los directores de orquesta. El promotor desempeña un papel vital en su interacción, controlando los marcapasos. Los resultados de este estudio se han publicado ahora en la revista "Nature Communications".
Ver la reacción en directo
"Muchos procesos químicos utilizan catalizadores en forma de minúsculas nanopartículas", explica el profesor Günther Rupprechter, del Instituto de Química de Materiales de la Universidad Técnica de Viena. Mientras que el rendimiento de los catalizadores puede determinarse fácilmente mediante el análisis de los productos, este enfoque no permite obtener información microscópica.
Esto ha cambiado ahora. A lo largo de varios años, Günther Rupprechter y su equipo han desarrollado sofisticados métodos que permiten observar directamente nanopartículas individuales durante una reacción química. Esto permite ver cómo cambia la actividad en distintos puntos de estas nanopartículas durante el transcurso de la reacción.
"Utilizamos nanotips de rodio que se comportan como nanopartículas", explica Günther Rupprechter. "Pueden servir de catalizadores, por ejemplo, cuando el hidrógeno y el oxígeno se combinan para formar moléculas de agua, la reacción que estamos examinando en detalle".
Oscilando entre lo "activo" y lo "inactivo
En los últimos años, el equipo de TU Wien ya demostró que distintas regiones de las superficies de las nanopartículas presentan comportamientos diferentes: oscilan entre un estado activo y otro inactivo. A veces, la reacción química deseada se produce en determinados lugares, mientras que otras veces no.
Utilizando microscopios específicos, se ha demostrado que en cada nanopartícula se producen varias oscilaciones de este tipo en paralelo, y que todas ellas se influyen mutuamente. Ciertas regiones de la superficie de la nanopartícula, a menudo de sólo unos pocos átomos de diámetro, desempeñan un papel más importante que otras: actúan como "marcapasos" muy eficaces, controlando incluso las oscilaciones químicas de otras regiones.
Los promotores pueden ahora interferir en este comportamiento marcapasos, y eso es precisamente lo que los métodos desarrollados en la TU Wien han permitido investigar a los investigadores. Cuando se utiliza rodio como catalizador, el lantano puede servir de promotor de las reacciones catalíticas. Se colocaron átomos individuales de lantano en la diminuta superficie de una nanopartícula de rodio. La misma partícula se investigó tanto en presencia como en ausencia del promotor. Este método reveló en detalle el efecto específico de los átomos individuales de lantano sobre el progreso de la reacción química.
El lantano lo cambia todo
Maximilian Raab, Johannes Zeininger y Carla Weigl han realizado los experimentos. "La diferencia es enorme", afirma Maximilian Raab. "Un átomo de lantano puede unirse al oxígeno, y eso cambia la dinámica de la reacción catalítica". La minúscula cantidad de lantano altera el acoplamiento entre distintas zonas de la nanopartícula.
"El lantano puede desactivar selectivamente ciertos marcapasos", explica Johannes Zeininger. "Imaginemos una orquesta con dos directores: oiríamos una música bastante compleja. El promotor se encarga de que sólo quede un marcapasos, simplificando y ordenando la situación".
Además de las mediciones, el equipo, apoyado por Alexander Genest y Yuri Suchorski, desarrolló un modelo matemático para simular el acoplamiento entre las áreas individuales de la nanopartícula. Este enfoque ofrece una forma de describir la catálisis química más poderosa que antes: no sólo basada en la entrada y la salida, sino en un modelo complejo que considera cómo las distintas zonas del catalizador cambian entre actividad e inactividad y, controladas por promotores, se influyen mutuamente.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
























































