En experimentos em ratones, virus del Zika elimina un tumor cerebral humano común en niños
Ensayo pre-clínico abre la puerta al uso terapéutico del virus
Un estudio publicado en Cancer Research, de la Asociación Americana para la Investigación del cáncer, revela el lado terapéutico del virus del Zika que, en 2015, puso en alerta a las autoridades mundiales de salud pública, al establecerse un vínculo causal entre la infección por el virus durante la gestación y el nacimiento de niños con microcefalia. Ahora, investigadores brasileños del Centro de Estudios del Genoma Humano y Células Tronco demuestran, por primera vez en animales, el efecto deletéreo de la inyección del virus purificado, en bajas concentraciones, sobre tumores embrionarios cerebrales, de células humanas, inducidos em ratones con baja inmunidad. El artículo se titula "Zika vírus selectively kills aggressive human embryonal CNS tumor cells in vitro and in vivo".
El artículo describe experimentos donde fueron utilizadas, entre otras, líneas celulares humanas derivadas de dos tipos de tumores embrionarios del sistema nervioso central (SNC): meduloblastoma y tumor teratoide rabdoide atípico (AT/RT, en su sigla en inglés). Se trata de tumores que afectan principalmente a niños de menos de cinco años.
"Los tumores del SNC son los tumores sólidos más frecuentes en niños y adolescentes", explica Keith Okamoto, uno de los autores principales del estudio. "El pico de incidencia del meduloblastoma es en niños de 4 a 5 años de edad. O AT/RT tiene una mayor incidencia en niños aún más jóvenes, de menos de 2 años".
En 20 de 29 animales tratados con el virus del Zika en el estudio, los tumores remitieron. En siete de ellos (cinco con AT/RT e dos con meduloblastoma), la remisión fue completa: el tumor desapareció. En algunos casos, el virus también fue efectivo contra las metástasis - o bien eliminando el tumor secundario o inhibiendo su desarrollo.
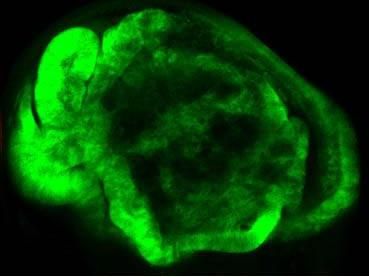
Efecto del virus del Zika sobre tumores en el cerebro y en la espina dorsal. Las células tumorales se encuentran modificadas para emitir luz, que puede ser captada con un equipo, produciendo una señal coloreada en el lugar donde se encuentran los tumores. Las imágenes muestran la evolución de los tumores después de la inyección del virus (Ti).
Mayana Zatz, coordinadora del centro y una de las autoras principales del estudio, no duda en clasificar los resultados de "espectaculares". El próximo paso será tratar de encontrar colaboradores para lo que se llama en la jerga médica "fase 1", y que será realizada en personas, niños en este caso. Esa es una de las causas del entusiasmo que transmite Mayana, y que ella procura contener.
"Vamos a tener que aguantar la ansiedad y no poner el carro delante de los bueyes. Es muy importante que empecemos con dos o tres pacientes y, si el virus funciona, ir ampliando ese número".
Para eso será necesario obtener el virus purificado en mayores cantidades, y producido de acuerdo con las buenas prácticas de cultivo exigidas para pruebas en seres humanos. Esta etapa está siendo llevada a cabo con el Instituto Butantan, que ya produjo los virus empleados en el presente estudio. A partir de ahí será posible crear un protocolo para su aplicación en pacientes.
Carolini Kaid, doctoranda del Centro de Estudios del Genoma Humano orientada por Keith Okamoto, es la primera autora del trabajo. Kaid se responsabilizó especialmente por los animales: realizó las cirugías para implantar los tumores, inyectó el virus del Zika y acompañó la evolución de los animales.
Nota diez en seguridad
Garantizar que el virus es seguro es crucial para llevar las observaciones del estudio a la clínica. En este sentido, los resultados del artículo son prometedores. Concentraciones de una partícula viral por cada diez células fueron suficientes para infectar y matar células derivadas de tumores de AT/RT y meduloblastoma. Además, el virus mostró gran especificidad por ese tipo de células.
"El virus no infectó células tumorales indiscriminadamente," explica Okamoto. "Es bastante específico para células tumorales del sistema nervioso". Tampoco infectó neuronas ya diferenciadas, lo que representaría una gran ventaja en el contexto clínico. Los investigadores también testaron in vitro la capacidad infectiva de los virus formados en las células tumorales después de la infección. Los resultados muestran que esas nuevas partículas virales son defectuosas, lo que evitaría la expansión descontrolada del virus en el cuerpo del paciente después del tratamiento antitumoral.
Durante la epidemia de 2015, miles de personas fueron infectadas con el virus del Zika. A pesar de eso, la mayoría de los pacientes, niños y adultos, permanecieron asintomáticos. Solo una pequeña proporción de las personas infectadas desarrolló condiciones graves, como el síndrome de Guillain-Barré o encefalitis. Estas observaciones son muy importantes cuando se trata de evaluar los riesgos y la seguridad de un nuevo tratamiento.
"Existe una perspectiva muy positiva", dice Okamoto. "Pero todavía tenemos un camino a recorrer para poder avanzar de forma segura hacia la parte clínica."