Nueva función para enzima vegetal podría llevar a la química verde
El descubrimiento puede inspirar el desarrollo de mejores catalizadores industriales
Científicos del Laboratorio Nacional Brookhaven del Departamento de Energía de los Estados Unidos han descubierto una nueva función en una enzima vegetal que podría tener implicaciones para el diseño de nuevos catalizadores químicos. La enzima cataliza, o inicia, una de las reacciones químicas fundamentales necesarias para sintetizar una amplia gama de moléculas orgánicas, incluyendo las que se encuentran en los lubricantes, cosméticos y las que se utilizan como materias primas para la fabricación de plásticos.

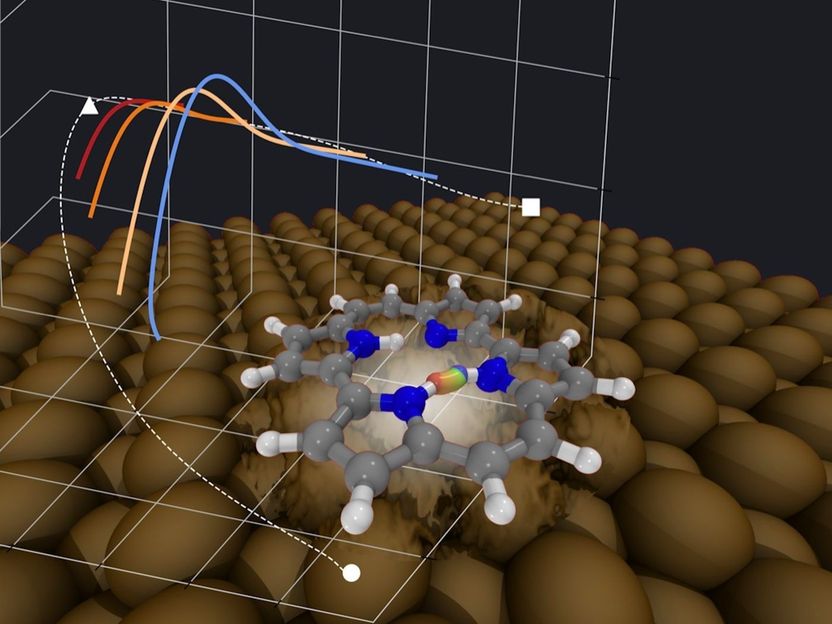
El bioquímico del Brookhaven Lab John Shanklin con Ed Whittle, asociado jubilado de biología, mostrando una imagen estructural de una enzima desaturasa que introduce grupos hidroxilos adyacentes en un ácido graso. Este ácido graso puede utilizarse para sintetizar una amplia gama de moléculas orgánicas, por lo que el descubrimiento de la enzima vegetal puede inspirar el desarrollo de nuevos catalizadores industriales "más ecológicos".
Brookhaven National Laboratory
"Esta enzima podría inspirar una nueva forma de química'verde'", dijo el bioquímico del Brookhaven Lab John Shanklin, quien dirigió la investigación. "Tal vez podamos adaptar esta biomolécula para hacer químicos útiles en las plantas, o usarla como base para diseñar nuevos catalizadores bio-inspirados para reemplazar los catalizadores más caros y tóxicos que se usan actualmente".
El equipo hizo el descubrimiento en el curso de su investigación en curso sobre las enzimas que desaturan los aceites vegetales. Estas enzimas desaturasas separan los átomos de hidrógeno de los átomos de carbono adyacentes específicos en una cadena de hidrocarburos e insertan un enlace doble entre esos átomos de carbono. El grupo de Shanklin había creado previamente una versión triple mutante de una enzima desaturasa con propiedades interesantes, y estaban estudiando las tres mutaciones por separado para ver qué hacía cada una.
Dos de las enzimas mutantes simples resultaron eliminar el doble enlace entre los átomos de carbono adyacentes y añadieron un "OH" (grupo hidroxilo) a cada carbono para producir un ácido graso con dos grupos hidroxilo adyacentes.
Los ácidos grasos que contienen estos grupos OH adyacentes, conocidos como dioles, son componentes químicos importantes para la fabricación de lubricantes, como los que mantienen los motores calientes funcionando sin problemas. También pueden convertirse en bloques de construcción para la fabricación de plásticos u otros productos básicos.
"Los dioles son químicos industriales muy importantes, pero fabricarlos artificialmente en el laboratorio es bastante problemático", señaló Shanklin.
Los mejores catalizadores industriales para esta reacción son caros, altamente volátiles y tóxicos, anotó.
Otro problema es que hay distintas formas de dioles, y es difícil para los químicos hacer una sola forma pura.
"Los mutantes enzimáticos que descubrimos de forma natural forman una sola forma, por lo que están listos para su uso sin necesidad de procesamiento adicional ni desperdicio", dijo Shanklin.
El rastreo de los orígenes de los átomos de oxígeno en los dos grupos OH reveló que ambos provenían de la misma molécula de oxígeno (O2). La capacidad de transferir ambos átomos de oxígeno de una sola molécula de O2 durante una reacción, conocida como química de la "dioxigenasa", fue una sorpresa para una enzima "diiron" (una con dos átomos de hierro en su sitio activo).
"La química de la dioxinasa no ha sido reportada previamente para las enzimas de dihierro", dijo Shanklin. "Tuvimos que realizar algunos experimentos técnicamente desafiantes para proporcionar pruebas irrefutables de que esto estaba sucediendo, y sin la creatividad y tenacidad de Ed Whittle, no hubiéramos completado este estudio".
Whittle, el autor principal del artículo (ahora retirado del Brookhaven Lab), ha trabajado diligentemente en este proyecto durante un período de años en el laboratorio de Shanklin para concretar este importante nuevo descubrimiento.
La próxima meta del equipo es obtener una estructura cristalina de esta enzima usando rayos X en la Fuente de Luz Nacional de Sincrotrón II (NSLS-II), una instalación de usuario de la Oficina de Ciencia del DOE en el Laboratorio Brookhaven.
"Compartiremos esa información estructural con nuestros colegas de química computacional para averiguar los detalles de cómo esta química sin precedentes puede ocurrir con esta clase de catalizador."
Ese trabajo podría ayudar al equipo a aprender a controlar la configuración de los catalizadores hechos en laboratorio para imitar la versión derivada de la planta.
"Si podemos incorporar lo que hemos aprendido en el diseño de catalizadores industriales, esas reacciones podrían producir productos más puros con menos residuos y evitar el uso de productos químicos tóxicos", dijo Shanklin.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.