Combinar la luz solar y el nitrato de las aguas residuales para fabricar el segundo producto químico del mundo
Ingenieros de la UIC convierten los nitratos en amoníaco en una reacción electroquímica sostenible con una alta eficiencia de conversión de energía solar en combustible
Ingenieros de la Universidad de Illinois Chicago han creado una reacción electroquímica alimentada por energía solar que no sólo utiliza las aguas residuales para fabricar amoníaco -el segundo producto químico más producido del mundo-, sino que además consigue una eficiencia de conversión de energía solar en combustible 10 veces mejor que cualquier otra tecnología comparable.

Investigadores de la UIC crean un sistema electroquímico sostenible en el que una célula solar se acopla a un pozo que contiene una solución líquida. Cuando se carga, los nitratos de las aguas residuales de la solución líquida se convierten en amoníaco.
Meenesh Singh/UIC
"Esta tecnología y nuestro método tienen un gran potencial para permitir la síntesis de fertilizantes a la carta y podrían tener un impacto inmenso en los sectores agrícola y energético de los países desarrollados y en vías de desarrollo, así como en los esfuerzos por reducir los gases de efecto invernadero procedentes de los combustibles fósiles", afirma el investigador principal, Meenesh Singh, profesor adjunto de Ingeniería Química en la Facultad de Ingeniería de la UIC.
El amoníaco, una combinación de un átomo de nitrógeno y tres de hidrógeno, es un compuesto clave de los fertilizantes y de muchos productos manufacturados, como los plásticos y los productos farmacéuticos. Los métodos actuales para fabricar amoníaco a partir de nitrógeno requieren enormes cantidades de calor, generadas por la quema de combustibles fósiles, para romper los fuertes enlaces entre los átomos de nitrógeno y que puedan unirse al hidrógeno. Este proceso centenario produce una fracción sustancial de las emisiones mundiales de gases de efecto invernadero, que son una fuerza impulsora del cambio climático.
Anteriormente, Singh y sus colegas desarrollaron un método respetuoso con el medio ambiente para fabricar amoníaco filtrando gas nitrógeno puro a través de un tamiz de malla cubierto de catalizador y cargado eléctricamente en una solución acuosa. Esta reacción sólo utilizaba una ínfima cantidad de energía fósil para electrificar la malla, que rompe los átomos de nitrógeno, pero producía más gas hidrógeno (80%) que amoníaco (20%).
Ahora, los investigadores han mejorado este concepto y han desarrollado un nuevo método que utiliza el nitrato, uno de los contaminantes más comunes de las aguas subterráneas, para suministrar nitrógeno y la luz solar para electrificar la reacción. El sistema produce casi el 100% de amoníaco con casi cero reacciones secundarias de gas hidrógeno. La reacción no necesita combustibles fósiles y no produce dióxido de carbono ni otros gases de efecto invernadero, y su uso de la energía solar produce una eficiencia solar-combustible sin precedentes, o STF, del 11%, que es 10 veces mejor que cualquier otro sistema de vanguardia para producir amoníaco (alrededor del 1% de STF).
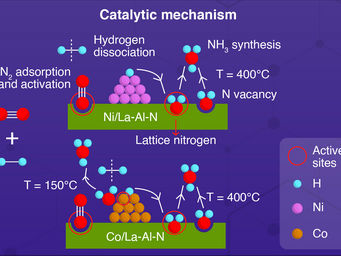
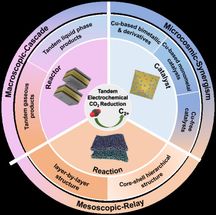
El nuevo método se basa en un catalizador de cobalto, que los investigadores describen junto con el nuevo proceso en su artículo "Solar-Driven Electrochemical Synthesis of Ammonia using Nitrate with 11% Solar-to-Fuel Efficiency at Ambient Conditions".
Para identificar el catalizador, los investigadores aplicaron primero la teoría computacional para predecir qué metal funcionaría mejor. Tras identificar el cobalto a través de estos modelos, el equipo experimentó con el metal, probando diferentes formas de optimizar su actividad en la reacción. Los investigadores descubrieron que una superficie rugosa de cobalto derivada de la oxidación era la que mejor funcionaba para crear una reacción selectiva, es decir, que convertía casi todas las moléculas de nitrato en amoníaco.
"Encontrar un catalizador activo, selectivo y estable que funcione en un sistema alimentado por energía solar es una poderosa prueba de que la síntesis sostenible de amoníaco a escala industrial es posible", dijo Singh.
La reacción no sólo es neutra en carbono, lo que es bueno para el medio ambiente, sino que, si el sistema se desarrolla para su uso industrial, también puede tener un efecto casi negativo y restaurador en el medio ambiente.
"Utilizar el nitrato de las aguas residuales significa que también tenemos que eliminar el contaminante de las aguas superficiales y subterráneas. Con el tiempo, esto significa que el proceso puede ayudar simultáneamente a corregir los residuos industriales y las aguas de escorrentía y a reequilibrar el ciclo del nitrógeno, sobre todo en las zonas rurales que pueden sufrir desventajas económicas o que corren el mayor riesgo por la alta exposición al exceso de nitrato", dijo Singh.
La elevada exposición a los nitratos a través del agua potable se ha asociado a problemas de salud como el cáncer, las enfermedades tiroideas, los partos prematuros y el bajo peso al nacer.
"Todos estamos muy emocionados con este logro, y no nos detenemos aquí. Esperamos tener pronto un prototipo más grande con el que podamos hacer pruebas a una escala mucho mayor", dijo Singh, que ya está colaborando con corporaciones municipales, centros de tratamiento de aguas residuales y otras empresas del sector para seguir desarrollando el sistema.
La Oficina de Gestión Tecnológica de la UIC ha presentado una patente para el nuevo proceso.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.