Las moléculas de agua líquida son intrínsecamente asimétricas
Nuevos conocimientos sobre los enlaces entre la molécula de agua
Los icebergs flotan sobre el agua porque el agua líquida subyacente tiene una densidad superior a la del iceberg. El agua líquida tiene su mayor densidad a 4 °C, una de las llamadas anomalías del agua, es decir, propiedades de los líquidos que raramente se observan en otros líquidos.
El origen de estas anomalías es objeto de investigación científica desde hace mucho tiempo. Los investigadores del Instituto Max Planck de Investigación de Polímeros han descubierto ahora otra pieza del rompecabezas para explicar el comportamiento especial del agua.
Muchas de las propiedades anómalas del agua se deben a las interacciones especiales entre las moléculas de agua, los llamados enlaces de hidrógeno. Cada molécula de agua puede donar dos de estos enlaces -uno de cada átomo de hidrógeno- y aceptar dos de otras moléculas vecinas. A diferencia del hielo, en el agua líquida estos enlaces se rompen y se vuelven a formar una media de 1 billón de veces por segundo, lo que permite que las moléculas de agua se agrupen y se muevan con gran rapidez. Debido al rápido movimiento de las moléculas de agua en el líquido, cabría suponer que la fuerza de los enlaces individuales con sus vecinas es puramente aleatoria.
Sin embargo, el equipo dirigido por el jefe de grupo Johannes Hunger ha descubierto que las distancias de los enlaces de hidrógeno no son simplemente aleatorias, sino que dos enlaces de una molécula tienen distinta fuerza: si un enlace es muy fuerte -es decir, la primera molécula de agua vecina está muy cerca-, el segundo enlace de hidrógeno es débil -es decir, la segunda molécula de agua vecina está más lejos-.
Esta alternancia en las distancias de enlace conduce a la estructuración del líquido nominalmente desordenado: si se pasa de una molécula de agua a la siguiente y a la que le sigue, siempre hay una molécula vecina fuertemente enlazada. Como resultado, en el líquido pueden formarse estructuras como anillos o cadenas de moléculas de agua. Por tanto, la estructura del agua líquida no es una mera disposición aleatoria de moléculas de agua individuales, sino que sigue ciertas reglas.
Para obtener estos resultados, los científicos diluyeron el agua con un disolvente para poder examinar moléculas de agua aisladas. Hicieron vibrar átomos individuales de las moléculas de agua con ayuda de láseres e investigaron cómo se influían mutuamente las vibraciones. Esto les permitió medir la fuerza de los enlaces de hidrógeno individuales y la fuerza del enlace vecino al mismo tiempo.
El estudio, que acaba de publicarse en la revista "Nature Communications", contribuye a comprender mejor las anomalías del agua a nivel molecular.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Más noticias del departamento ciencias

Reciba la química en su bandeja de entrada
Al enviar el formulario, se muestra usted de acuerdo con que LUMITOS AG le envíe por correo electrónico el boletín o boletines seleccionados anteriormente. Sus datos no se facilitarán a terceros. El almacenamiento y el procesamiento de sus datos se realiza sobre la base de nuestra política de protección de datos. LUMITOS puede ponerse en contacto con usted por correo electrónico a efectos publicitarios o de investigación de mercado y opinión. Puede revocar en todo momento su consentimiento sin efecto retroactivo y sin necesidad de indicar los motivos informando por correo postal a LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlín (Alemania) o por correo electrónico a revoke@lumitos.com. Además, en cada correo electrónico se incluye un enlace para anular la suscripción al boletín informativo correspondiente.
Noticias más leídas
Más noticias de nuestros otros portales
Contenido visto recientemente
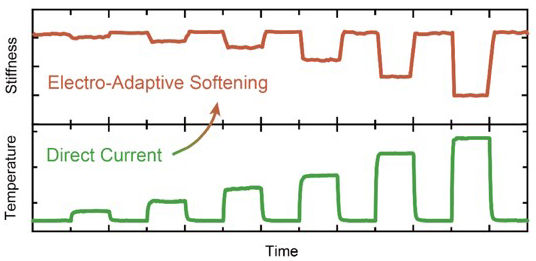
Un nanopapel muy fino que cambia de firme a blando con sólo pulsar un botón - Las nanofibrilas de celulosa bioinspiradas pueden ser controladas por la electricidad
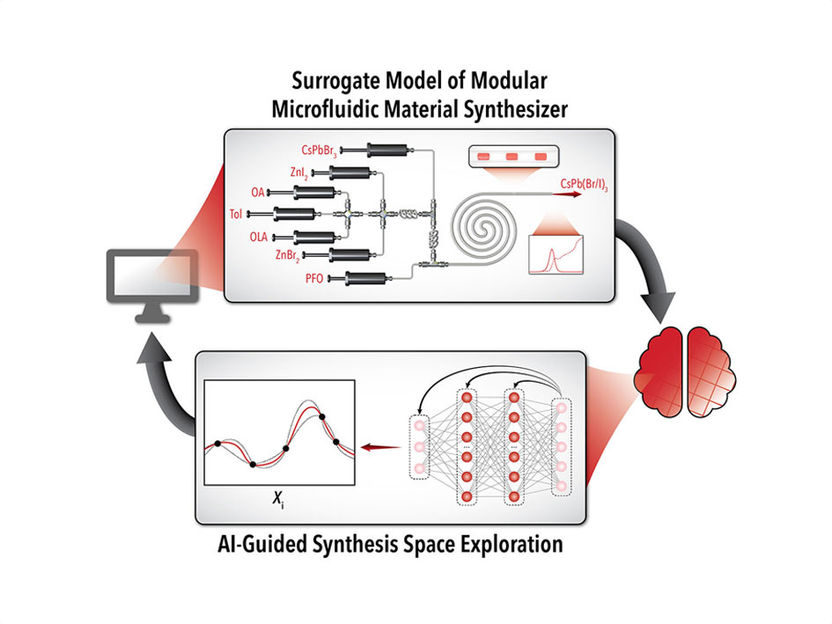
El laboratorio virtual encuentra la herramienta de IA adecuada para cada problema de química - "Los sistemas autónomos tienen un enorme potencial para acelerar la I+D y la fabricación de productos químicos"
Arcellinida



















































